Inflamación neurogénica, o NI, es el proceso fisiológico en el que los mediadores se descargan directamente de los nervios cutáneos para comenzar una respuesta inflamatoria. Esto da como resultado la creación de reacciones inflamatorias locales que incluyen eritema, hinchazón, aumento de la temperatura, sensibilidad y dolor. Finas fibras C somáticas aferentes no amielinadas, que responden a estímulos mecánicos y químicos de baja intensidad, son en gran parte responsables de la liberación de estos mediadores inflamatorios.
Cuando se estimulan, estas vías nerviosas en los nervios cutáneos liberan rápidamente neuropéptidos energéticos, o sustancia P y péptido relacionado con el gen de calcitonina (CGRP), en el microambiente, lo que desencadena una serie de respuestas inflamatorias. Hay una distinción importante en la inflamación inmunogénica, esa es la primera respuesta protectora y reparadora que hace el sistema inmune cuando un patógeno ingresa al cuerpo, mientras que la inflamación neurogénica implica una conexión directa entre el sistema nervioso y las respuestas inflamatorias. A pesar de que la inflamación neurogénica y la inflamación inmunológica pueden existir al mismo tiempo, los dos no son clínicamente indistinguibles. El objetivo del siguiente artículo es analizar el mecanismo de la inflamación neurogénica y el papel del sistema nervioso periférico en la defensa e inmunopatología del huésped.
Contenido
Inflamación neurogénica: el papel del sistema nervioso periférico en la defensa e inmunopatología del huésped
Resumen
Se piensa tradicionalmente que los sistemas periféricos nervioso e inmune cumplen funciones separadas. Sin embargo, esta línea se vuelve cada vez más borrosa por nuevos conocimientos sobre la inflamación neurogénica. Las neuronas nociceptores poseen muchas de las mismas vías de reconocimiento molecular para el peligro que las células inmunitarias y, en respuesta al peligro, el sistema nervioso periférico se comunica directamente con el sistema inmunitario, formando un mecanismo de protección integrado. La red de inervación densa de las fibras sensoriales y autonómicas en los tejidos periféricos y la alta velocidad de transducción neural permiten una modulación neurogénica local y sistémica rápida de la inmunidad. Las neuronas periféricas también parecen jugar un papel importante en la disfunción inmune en enfermedades autoinmunes y alérgicas. Por lo tanto, comprender la interacción coordinada de las neuronas periféricas con las células inmunes puede avanzar en los enfoques terapéuticos para aumentar la defensa del huésped y suprimir la inmunopatología.
Introducción
Hace dos mil años, Celsus definió la inflamación como la participación de cuatro signos cardinales: Dolor (dolor), Calor (calor), Rubor (enrojecimiento) y Tumor (hinchazón), una observación que indica que la activación del sistema nervioso se reconoció como parte integral de inflamación. Sin embargo, desde entonces se ha pensado principalmente en el dolor, solo como un síntoma y no como un participante en la generación de inflamación. En esta perspectiva, mostramos que el sistema nervioso periférico juega un papel directo y activo en la modulación de la inmunidad innata y adaptativa, de modo que los sistemas inmunológico y nervioso pueden tener una función protectora integrada común en la defensa del huésped y la respuesta a la lesión tisular, una intrincada interacción que también puede conducir a patología en enfermedades alérgicas y autoinmunes.
La supervivencia de los organismos depende fundamentalmente de la capacidad de montar una defensa contra el daño potencial del daño tisular y la infección. La defensa del huésped implica tanto un comportamiento de evitación para eliminar el contacto con un entorno peligroso (nocivo) (una función neural) como la neutralización activa de patógenos (una función inmunitaria). Tradicionalmente, el papel del sistema inmunológico en la lucha contra los agentes infecciosos y la reparación de la lesión tisular se ha considerado bastante distinto del del sistema nervioso, que transduce señales ambientales e internas dañinas en actividad eléctrica para producir sensaciones y reflejos (Fig.1). Proponemos que estos dos sistemas son en realidad componentes de un mecanismo de defensa unificado. El sistema nervioso somatosensorial está en una posición ideal para detectar el peligro. En primer lugar, todos los tejidos que están muy expuestos al entorno externo, como las superficies epiteliales de la piel, los pulmones, el tracto urinario y digestivo, están densamente inervados por nociceptores, fibras sensoriales de alto umbral que producen dolor. En segundo lugar, la transducción de estímulos externos nocivos es casi instantánea, órdenes de magnitud más rápida que la movilización del sistema inmunológico innato y, por lo tanto, puede ser el `` primer respondedor '' en la defensa del huésped.
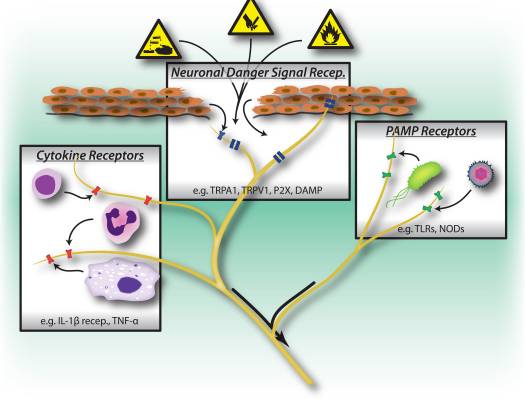
Figura 1: Los estímulos nocivos, las vías de reconocimiento microbiano e inflamatorio desencadenan la activación del sistema nervioso periférico. Las neuronas sensoriales poseen varios medios para detectar la presencia de estímulos nocivos / dañinos. 1) Los receptores de señales de peligro, incluidos los canales TRP, P2X y los receptores de patrón molecular asociado a peligros (DAMP) reconocen señales exógenas del entorno (por ejemplo, calor, acidez, productos químicos) o señales de peligro endógenas liberadas durante traumas / daños tisulares (p. ácido úrico, hidroxinonatos). 2) Los receptores de reconocimiento de patrón (PRR), como los receptores Toll-like (TLR) y Nod-like (NLR) reconocen patrones moleculares asociados a patógenos (PAMP) arrojados por bacterias o virus invasores durante la infección. 3) Los receptores de citocina reconocen los factores secretados por las células inmunitarias (p. Ej., IL-1beta, TNF-alfa, NGF), que activan las quinasas de los mapas y otros mecanismos de señalización para aumentar la excitabilidad de la membrana.
Además de las entradas ortodrómicas a la médula espinal y el cerebro desde la periferia, los potenciales de acción en las neuronas nociceptores también pueden transmitirse de forma antidrómica en los puntos de ramificación hacia la periferia, el reflejo axónico. Estos, junto con las despolarizaciones locales sostenidas, conducen a una liberación rápida y local de mediadores neuronales tanto de los axones periféricos como de las terminales (Fig. 2) 1. Los experimentos clásicos de Goltz (en 1874) y de Bayliss (en 1901) mostraron que las raíces dorsales estimulantes eléctricamente induce vasodilatación cutánea, lo que llevó al concepto de `` inflamación neurogénica '', independiente de la producida por el sistema inmunológico (fig.3).
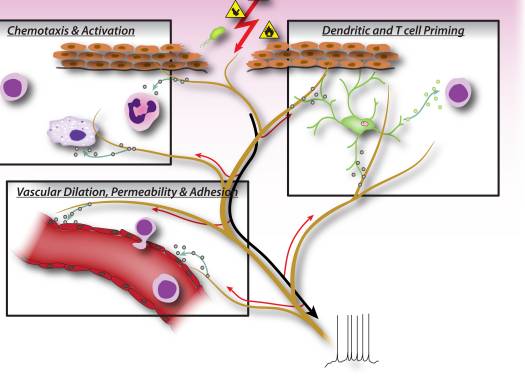
Figura 2: Los factores neuronales liberados por las neuronas sensoriales del nociceptores dirigen directamente la quimiotaxis de los leucocitos, la hemodinámica vascular y la respuesta inmune. Cuando los estímulos nocivos activan las señales aferentes en los nervios sensoriales, se generan reflejos antidrómicos del axón que inducen la liberación de neuropéptidos en los terminales periféricos de las neuronas. Estos mediadores moleculares tienen varias acciones inflamatorias: 1) Quimiotaxis y activación de neutrófilos, macrófagos y linfocitos en el sitio de la lesión y desgranulación de los mastocitos. 2) Señalización a las células endoteliales vasculares para aumentar el flujo sanguíneo, la fuga vascular y el edema. Esto también permite un reclutamiento más fácil de leucocitos inflamatorios. 3) Cebado de células dendríticas para dirigir la posterior diferenciación de células T auxiliares en los subtipos Th2 o Th17.

Figura 3: Cronología de los avances en la comprensión de los aspectos neurogénicos de la inflamación desde Celsus hasta la actualidad.
La inflamación neurogénica está mediada por la liberación de los neuropéptidos péptido relacionado con el gen de la calcitonina (CGRP) y la sustancia P (SP) de los nociceptores, que actúan directamente sobre las células del músculo liso y endotelial vascular 2�5. CGRP produce efectos de vasodilatación 2, 3, mientras que SP aumenta la permeabilidad capilar que conduce a la extravasación de plasma y edema 4, 5, contribuyendo al rubor, calor y tumor de Celsus. Sin embargo, los nociceptores liberan muchos neuropéptidos adicionales (base de datos en línea: www.neuropéptidos.nl/), que incluyen adrenomedulina, neuroquininas A y B, péptido intestinal vasoactivo (VIP), neuropéptido (NPY) y péptido liberador de gastrina (GRP), así como otros mediadores moleculares como glutamato, óxido nítrico (NO) y citocinas como eotaxina 6.
Ahora apreciamos que los mediadores liberados de las neuronas sensoriales en la periferia no solo actúan sobre la vasculatura, sino que también atraen y activan directamente las células inmunes innatas (mastocitos, células dendríticas) y las células inmunitarias adaptativas (linfocitos T) 7-12. En el contexto agudo de daño tisular, conjeturamos que la inflamación neurogénica es protectora, facilitando la cicatrización fisiológica de heridas y la defensa inmune contra patógenos al activar y reclutar células inmunes. Sin embargo, estas comunicaciones neuroinmunes también desempeñan probablemente un papel importante en la fisiopatología de las enfermedades alérgicas y autoinmunes al amplificar las respuestas inmunitarias patológicas o desadaptativas. En modelos animales de artritis reumatoide, por ejemplo, Levine y sus colegas han demostrado que la denervación de la articulación conduce a una notable atenuación de la inflamación, que depende de la expresión neuronal de la sustancia P 13, 14. En estudios recientes de inflamación alérgica de las vías respiratorias, colitis y psoriasis, las neuronas sensoriales primarias juegan un papel central en el inicio y aumento de la activación de la inmunidad innata y adaptativa 15-17.
Proponemos, por lo tanto, que el sistema nervioso periférico no solo desempeñe un papel pasivo en la defensa del huésped (detección de estímulos nocivos e iniciación del comportamiento de evitación), sino también un papel activo en concierto con el sistema inmunitario para modular las respuestas y combatir estímulos, un papel que puede subvertirse para contribuir a la enfermedad.
Caminos de reconocimiento de peligros compartidos en los sistemas nerviosos periféricos e innato
Las neuronas sensoriales periféricas están adaptadas para reconocer el peligro para el organismo en virtud de su sensibilidad a estímulos químicos intensos mecánicos, térmicos e irritantes (Fig. 1). Los canales iónicos del potencial del receptor transitorio (TRP) son los mediadores moleculares de nocicepción más estudiados, que conducen la entrada no selectiva de cationes tras la activación por diversos estímulos nocivos. TRPV1 se activa con altas temperaturas, pH bajo y capsaicina, el componente irritante vallinoide de chiles 18. TRPA1 interviene en la detección de sustancias químicas reactivas, incluidos irritantes ambientales como gas lacrimógeno e isotiocianatos industriales 19, pero lo que es más importante, también se activa durante la lesión tisular mediante señales moleculares endógenas, incluidas 4-hydroxynonenal y prostaglandinas 20, 21.
Curiosamente, las neuronas sensoriales comparten muchas de las mismas vías de receptores de reconocimiento molecular de patógenos y peligros que las células inmunes innatas, lo que les permite detectar también patógenos (Fig. 1). En el sistema inmune, los patógenos microbianos son detectados por los receptores de reconocimiento de patrones codificados por línea germinal (PRR), que reconocen patrones moleculares asociados a patógenos exógenos ampliamente conservados (PAMP). Los primeros PRR que se identificaron fueron miembros de la familia del receptor tipo toll (TLR), que se unen a la levadura, los componentes de la pared celular derivados de bacterias y el ARN viral 22. Después de la activación de PRR, se activan las vías de señalización aguas abajo que inducen la producción de citoquinas y la activación de la inmunidad adaptativa. Además de los TLR, las células inmunitarias innatas se activan durante la lesión tisular por señales de peligro derivadas endógenas, también conocidas como patrones moleculares asociados al daño (DAMP) o alarmin 23, 24. Estas señales de peligro incluyen HMGB1, ácido úrico y proteínas de choque térmico liberadas por las células que mueren durante la necrosis, activando las células inmunitarias durante las respuestas inflamatorias no infecciosas.
Los PRR, incluidos los TLR 3, 4, 7 y 9, son expresados por neuronas nociceptores, y la estimulación por ligandos TLR conduce a la inducción de corrientes de entrada y la sensibilización de los nociceptores a otros estímulos de dolor 25-27. Además, la activación de las neuronas sensoriales por el ligando de TLR7 imiquimod conduce a la activación de una vía sensorial específica del prurito 25. Estos resultados indican que el dolor y el prurito asociados a la infección pueden deberse en parte a la activación directa de las neuronas por factores derivados de patógenos, que a su vez activar las células inmunes mediante la liberación periférica de moléculas de señalización neuronal.
Uno de los principales DAMP / alarmina liberados durante la lesión celular es el ATP, que es reconocido por receptores purinérgicos tanto en las neuronas nociceptores como en las células inmunes 28-30. Los receptores purinérgicos se componen de dos familias: receptores P2X, canales catiónicos activados por ligandos y receptores P2Y, receptores acoplados a proteína G. En las neuronas nociceptores, el reconocimiento de ATP se produce a través de P2X3, lo que conduce a corrientes catiónicas que se densifican rápidamente y al dolor 28, 30 (fig.1), mientras que los receptores P2Y contribuyen a la activación de los nociceptores mediante la sensibilización de TRP y los canales de sodio dependientes de voltaje. En los macrófagos, la unión de ATP a los receptores P2X7 conduce a la hiperpolarización y la activación aguas abajo del inflamasoma, un complejo molecular importante en la generación de IL-1beta e IL-18 29. Por lo tanto, el ATP es una potente señal de peligro que activa tanto las neuronas periféricas como las innatas. inmunidad durante la lesión, y algunas evidencias incluso sugieren que las neuronas expresan partes de la maquinaria molecular del inflamasoma 31.
La otra cara de las señales de peligro en los nociceptores es el papel de los canales TRP en la activación de las células inmunitarias. TRPV2, un homólogo de TRPV1 activado por calor nocivo, se expresa a niveles elevados en células inmunes innatas 32. La ablación genética de TRPV2 condujo a defectos en la fagocitosis de macrófagos y eliminación de infecciones bacterianas 32. Los mastocitos también expresan canales TRPV, que pueden mediar directamente su desgranulación 33. Queda por determinar si las señales de peligro endógenas activan las células inmunitarias de manera similar a los nociceptores.
Un medio clave de comunicación entre las células inmunes y las neuronas nociceptores son las citocinas. Tras la activación de los receptores de citocinas, las vías de transducción de señales se activan en las neuronas sensoriales que conducen a la fosforilación aguas abajo de las proteínas de membrana, incluido el TRP y los canales dependientes de voltaje (Fig. 1). La sensibilización resultante de los nociceptores significa que los estímulos mecánicos y térmicos normalmente inocuos ahora pueden activar los nociceptores. La interleucina 1 beta y el TNF-alfa son dos importantes citocinas liberadas por las células inmunitarias innatas durante la inflamación. La IL-1beta y el TNF-alfa son detectados directamente por los nociceptores que expresan los receptores afines, inducen la activación de las cinasas del mapa de p38 que conducen a una mayor excitabilidad de la membrana 34-36. El factor de crecimiento nervioso (NGF) y la prostaglandina E (2) también son importantes mediadores inflamatorios liberados por las células inmunitarias que actúan directamente sobre las neuronas sensoriales periféricas para causar sensibilización. Un efecto importante de la sensibilización de los nociceptores por factores inmunes es una mayor liberación de neuropéptidos en terminales periféricos que activan aún más las células inmunes, induciendo así un ciclo de retroalimentación positiva que impulsa y facilita la inflamación.
Control del sistema nervioso sensorial de la inmunidad innata y adaptativa
En las primeras fases de la inflamación, las neuronas sensoriales envían señales a los mastocitos y células dendríticas residentes en el tejido, que son células inmunitarias innatas importantes para iniciar la respuesta inmunitaria (Fig. 2). Los estudios anatómicos han demostrado una aposición directa de los terminales con los mastocitos, así como con las células dendríticas, y los neuropéptidos liberados por los nociceptores pueden inducir la desgranulación o la producción de citocinas en estas células 7, 9, 37. Esta interacción juega un papel importante en las vías respiratorias alérgicas inflamación y dermatitis 10 12.
Durante la fase efectora de la inflamación, las células inmunitarias necesitan encontrar su camino hacia el sitio específico de la lesión. Muchos mediadores liberados de neuronas sensoriales, neuropéptidos, quimiocinas y glutamato, son quimiotácticos para neutrófilos, eosinófilos, macrófagos y células T, y mejoran la adhesión endotelial, lo que facilita la localización de las células inmunes 6, 38-41 (Fig. 2). Además, alguna evidencia implica que las neuronas pueden participar directamente en la fase efectora, ya que los propios neuropéptidos pueden tener funciones antimicrobianas directas 42.
Las moléculas de señalización derivadas de las neuronas también pueden dirigir el tipo de inflamación, contribuyendo a la diferenciación o especificación de diferentes tipos de células T inmunitarias adaptativas. Las células inmunitarias innatas fagocitan y procesan un antígeno, que luego migran al ganglio linfático más cercano y presentan el péptido antigénico a las células T vírgenes. Según el tipo de antígeno, las moléculas coestimuladoras de la célula inmunitaria innata y las combinaciones de citocinas específicas, las células T ingenuas maduran en subtipos específicos que sirven mejor al esfuerzo inflamatorio para eliminar el estímulo patógeno. Las células T CD4, o células T auxiliares (Th), se pueden dividir en cuatro grupos principales, Th1, Th2, Th17 y células T reguladoras (Treg). Las células Th1 están involucradas principalmente en la regulación de las respuestas inmunes a microorganismos intracelulares y enfermedades autoinmunes específicas de órganos; Th2 son fundamentales para la inmunidad contra patógenos extracelulares, como los helmintos, y son responsables de enfermedades alérgicas inflamatorias; Las células Th17 desempeñan un papel central en la protección contra los desafíos microbianos, como bacterias y hongos extracelulares; Las células Treg participan en el mantenimiento de la tolerancia propia y en la regulación de las respuestas inmunitarias. Este proceso de maduración de las células T parece estar fuertemente influenciado por mediadores neuronales sensoriales. Los neuropéptidos, como CGRP y VIP, pueden sesgar las células dendríticas hacia una inmunidad de tipo Th2 y reducir la inmunidad de tipo Th1 al promover la producción de ciertas citocinas e inhibir otras, así como al reducir o mejorar la migración de células dendríticas a los ganglios linfáticos locales 8 , 10, 43. Las neuronas sensoriales también contribuyen considerablemente a la inflamación alérgica (principalmente impulsada por Th2) 17. Además de regular las células Th1 y Th2, otros neuropéptidos, como SP y Hemoquinina-1, pueden impulsar la respuesta inflamatoria más hacia Th17 o Treg 44, 45, lo que significa que las neuronas también pueden participar en la regulación de la resolución inflamatoria. En inmunopatologías como la colitis y la psoriasis, el bloqueo de mediadores neuronales como la sustancia P puede amortiguar significativamente el daño mediado por el sistema inmunitario y las células T 15-17, aunque el antagonismo de un mediador puede por sí solo tener un efecto limitado sobre la inflamación neurogénica.
Teniendo en cuenta que las moléculas de señalización liberadas de las fibras nerviosas sensoriales periféricas regulan no solo los vasos sanguíneos pequeños, sino también la quimiotaxis, el desplazamiento, la maduración y la activación de las células inmunes, está claro que las interacciones neuroinmunes son mucho más intrincadas de lo que se pensaba (Fig. 2). Además, es bastante concebible que no se trate de mediadores neurales individuales sino de combinaciones específicas de moléculas de señalización liberadas de nociceptores que influyen en diferentes etapas y tipos de respuestas inmunes.
Control reflejo autónomo de la inmunidad
También parece prominente el papel de un circuito `` reflejo '' del sistema nervioso autónomo colinérgico en la regulación de las respuestas inmunitarias periféricas 46. El nervio vago es el principal nervio parasimpático que conecta el tronco del encéfalo con los órganos viscerales. El trabajo de Kevin Tracey y otros apuntan a potentes respuestas antiinflamatorias generalizadas en el choque séptico y la endotoxemia, desencadenadas por una actividad del nervio vago eferente que conduce a una supresión de los macrófagos periféricos 47-49. El vago activa las neuronas adrenérgicas periféricas del ganglio celíaco que inervan el bazo, lo que lleva a la liberación de acetilcolina, que se une a los receptores nicotínicos alfa-7 en los macrófagos del bazo y el tracto gastrointestinal. Esto induce la activación de la vía de señalización JAK2 / STAT3 SOCS3, que suprime poderosamente la transcripción de TNF-alfa 47. El ganglio celíaco adrenérgico también se comunica directamente con un subconjunto de células T de memoria productoras de acetilcolina, que suprimen los macrófagos inflamatorios 48.
Las células T asesinas naturales invariantes (iNKT) son un subconjunto especializado de células T que reconocen lípidos microbianos en el contexto de CD1d en lugar de antígenos peptídicos. Las células NKT son una población clave de linfocitos implicada en el combate de patógenos infecciosos y la regulación de la inmunidad sistémica. Las células NKT residen y trafican principalmente a través de la vasculatura y los sinusoides del bazo y el hígado. Los nervios beta-adrenérgicos simpáticos en el hígado señalizan directamente para modular la actividad de las células NKT 50. Durante un modelo de accidente cerebrovascular de ratón (MCAO), por ejemplo, la movilidad de células NKT hepáticas se suprimió visiblemente, que se revirtió por denervación simpática o antagonistas beta-adrenérgicos. Además, esta actividad inmunosupresora de las neuronas noradrenérgicas en células NKT condujo a aumentos en la infección sistémica y lesión pulmonar. Por lo tanto, las señales eferentes de las neuronas autónomas pueden mediar en una potente inmunosupresión.

Información del Dr. Alex Jiménez
La inflamación neurogénica es una respuesta inflamatoria local generada por el sistema nervioso. Se cree que juega un papel fundamental en la patogénesis de una variedad de problemas de salud, que incluyen migraña, psoriasis, asma, fibromialgia, eccema, rosácea, distonía y sensibilidad química múltiple. Aunque la inflamación neurogénica asociada con el sistema nervioso periférico ha sido ampliamente investigada, el concepto de inflamación neurogénica dentro del sistema nervioso central aún necesita más investigación. De acuerdo con varios estudios de investigación, sin embargo, se cree que las deficiencias de magnesio son la principal causa de inflamación neurogénica. El siguiente artículo muestra una descripción general de los mecanismos de la inflamación neurogénica en el sistema nervioso, que puede ayudar a los profesionales de la salud a determinar el mejor enfoque de tratamiento para una variedad de problemas de salud asociados con el sistema nervioso.
Conclusiones
¿Cuáles son las funciones específicas respectivas de los sistemas nerviosos somatosensorial y autónomo en la regulación de la inflamación y el sistema inmunológico (Fig. 4)? La activación de los nociceptores conduce a reflejos axónicos locales, que reclutan y activan localmente células inmunes y, por lo tanto, son principalmente proinflamatorios y espacialmente confinados. Por el contrario, la estimulación autónoma conduce a una inmunosupresión sistémica al afectar a los grupos de células inmunes en el hígado y el bazo. Los mecanismos de señalización aferente en la periferia que conducen a la activación del circuito reflejo colinérgico vagal inmunosupresor son poco conocidos. Sin embargo, el 80-90% de las fibras vagales son fibras sensoriales aferentes primarias y, por lo tanto, las señales de las vísceras, muchas potencialmente impulsadas por células inmunitarias, pueden conducir a la activación de interneuronas en el tronco del encéfalo y, a través de ellas, a una salida en las fibras vagales eferentes 46.
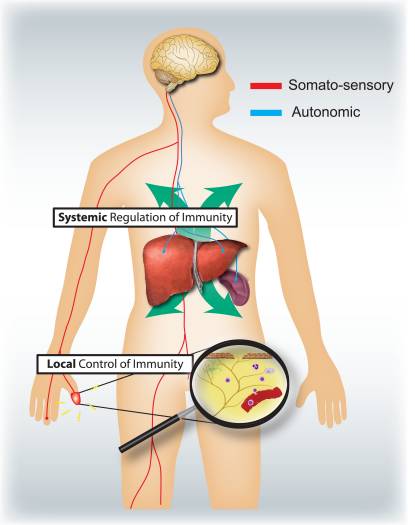
Figura 4: Los sistemas nerviosos sensoriales y autónomos modulan la respuesta inmune local y sistémica, respectivamente. Los nociceptores que inervan las superficies epiteliales (p. Ej., Piel y pulmón) inducen respuestas inflamatorias localizadas, activan los mastocitos y las células dendríticas. En la inflamación de las vías respiratorias alérgicas, la dermatitis y la artritis reumatoide, las neuronas nociceptores desempeñan un papel en la conducción de la inflamación. Por el contrario, los circuitos autónomos que inervan los órganos viscerales (p. Ej., Bazo e hígado) regulan la respuesta inmune sistémica bloqueando la activación de los macrófagos y las células NKT. En el accidente cerebrovascular y la endotoxemia séptica, estas neuronas desempeñan un papel inmunosupresor.
Típicamente, el curso del tiempo y la naturaleza de la inflamación, ya sea durante la infección, reacciones alérgicas o patologías autoinmunes, se define por las categorías de células inmunes involucradas. Será importante saber qué diferentes tipos de células inmunes están reguladas por señales sensoriales y autonómicas. Una evaluación sistemática de qué mediadores pueden ser liberados de nociceptores y neuronas autónomas y la expresión de receptores para estos por diferentes células inmunitarias innatas y adaptativas podría ayudar a abordar esta cuestión.
Durante la evolución, se han desarrollado vías moleculares de detección de peligros similares tanto para la inmunidad innata como para la nocicepción, a pesar de que las células tienen linajes de desarrollo completamente diferentes. Si bien los inmunólogos y neurobiólogos estudian por separado los PRR y los canales iónicos activados por ligandos nocivos, la línea entre estos dos campos es cada vez más borrosa. Durante el daño tisular y la infección patógena, es probable que la liberación de señales de peligro conduzca a una activación coordinada de neuronas periféricas y células inmunes con una comunicación bidireccional compleja y una defensa integrada del huésped. El posicionamiento anatómico de los nociceptores en la interfaz con el entorno, la velocidad de la transducción neural y su capacidad para liberar potentes cócteles de mediadores que actúan inmunológicamente permiten que el sistema nervioso periférico module activamente la respuesta inmunitaria innata y coordine la inmunidad adaptativa aguas abajo. Por el contrario, los nociceptores son muy sensibles a los mediadores inmunitarios, que activan y sensibilizan las neuronas. La inflamación neurogénica e inmunomediada no son, por tanto, entidades independientes, sino que actúan juntas como dispositivos de alerta temprana. Sin embargo, el sistema nervioso periférico también juega un papel importante en la fisiopatología, y quizás la etiología, de muchas enfermedades inmunes como el asma, la psoriasis o la colitis porque su capacidad para activar el sistema inmunológico puede amplificar la inflamación patológica 15-17. El tratamiento de los trastornos inmunitarios puede necesitar incluir, por lo tanto, la selección de los nociceptores y de las células inmunitarias.
Agradecimientos
Agradecemos al NIH por su apoyo (2R37NS039518).
En conclusión,`` Comprender el papel de la inflamación neurogénica en lo que respecta a la defensa del huésped y la inmunopatología es esencial para determinar el enfoque de tratamiento adecuado para una variedad de problemas de salud del sistema nervioso. Al observar las interacciones de las neuronas periféricas con las células inmunitarias, los profesionales de la salud pueden avanzar en los enfoques terapéuticos para ayudar a aumentar las defensas del huésped y suprimir la inmunopatología. El propósito del artículo anterior es ayudar a los pacientes a comprender la neurofisiología clínica de la neuropatía, entre otros problemas de salud relacionados con las lesiones nerviosas. Información a la que se hace referencia del Centro Nacional de Información Biotecnológica (NCBI). El alcance de nuestra información se limita a la quiropráctica, así como a las lesiones y afecciones de la columna. Para discutir el tema, no dude en preguntarle al Dr. Jiménez o contáctenos en 915-850-0900 .
Comisariada por el Dr. Alex Jiménez
Temas adicionales: Dolor de espalda
El dolor de espalda es una de las causas más frecuentes de discapacidad y días perdidos en el trabajo en todo el mundo. Como cuestión de hecho, el dolor de espalda se ha atribuido como la segunda razón más común para las visitas al consultorio médico, superado en número solo por las infecciones de las vías respiratorias superiores. Aproximadamente el 80% de la población experimentará algún tipo de dolor de espalda al menos una vez a lo largo de su vida. La columna vertebral es una estructura compleja compuesta por huesos, articulaciones, ligamentos y músculos, entre otros tejidos blandos. Debido a esto, lesiones y / o condiciones agravadas, como hernias discales, eventualmente puede conducir a síntomas de dolor de espalda. Las lesiones deportivas o las lesiones por accidentes automovilísticos suelen ser la causa más frecuente de dolor de espalda; sin embargo, a veces los movimientos más simples pueden tener resultados dolorosos. Afortunadamente, las opciones de tratamiento alternativo, como la atención quiropráctica, pueden ayudar a aliviar el dolor de espalda mediante el uso de ajustes espinales y manipulaciones manuales, mejorando finalmente el alivio del dolor.

TEMA EXTRA IMPORTANTE: Manejo del dolor lumbar
MÁS TEMAS: EXTRA EXTRA: Dolor crónico y tratamientos
Blanco
Referencias
Acordeón cercano
Alcance de la práctica profesional *
La información aquí contenida en "El papel de la inflamación neurogénica" no pretende reemplazar una relación personal con un profesional de la salud calificado o un médico con licencia y no es un consejo médico. Lo alentamos a que tome decisiones de atención médica basadas en su investigación y asociación con un profesional de la salud calificado.
Información del blog y debates sobre el alcance
Nuestro alcance informativo se limita a la quiropráctica, musculoesquelética, medicina física, bienestar, contribuyendo etiológico alteraciones viscerosomáticas dentro de las presentaciones clínicas, la dinámica clínica del reflejo somatovisceral asociado, los complejos de subluxación, los problemas de salud delicados y/o los artículos, temas y debates de medicina funcional.
Brindamos y presentamos colaboración clínica con especialistas de diversas disciplinas. Cada especialista se rige por su ámbito de práctica profesional y su jurisdicción de licencia. Utilizamos protocolos funcionales de salud y bienestar para tratar y apoyar la atención de lesiones o trastornos del sistema musculoesquelético.
Nuestros videos, publicaciones, temas, asuntos e ideas cubren cuestiones clínicas, problemas y temas que se relacionan y respaldan directa o indirectamente nuestro ámbito de práctica clínica.*
Nuestra oficina ha intentado razonablemente proporcionar citas de apoyo y ha identificado el estudio o los estudios de investigación relevantes que respaldan nuestras publicaciones. Proporcionamos copias de los estudios de investigación de respaldo disponibles para las juntas reguladoras y el público a pedido.
Entendemos que cubrimos asuntos que requieren una explicación adicional de cómo puede ayudar en un plan de atención o protocolo de tratamiento en particular; por lo tanto, para discutir más a fondo el tema anterior, no dude en preguntar Dr. Alex Jiménez, DC, o póngase en contacto con nosotros en 915-850-0900.
Estamos aquí para ayudarlo a usted y a su familia.
Bendiciones
El Dr. Alex Jimenez corriente continua MSACP, enfermero*, CCCT, IFMCP*, CIFM*, ATN*
email: coach@elpasomedicinafuncional.com
Licenciado como Doctor en Quiropráctica (DC) en Texas & New Mexico*
Número de licencia de Texas DC TX5807, Nuevo México DC Número de licencia NM-DC2182
Licenciada como enfermera registrada (RN*) in Florida
Licencia de Florida Licencia de RN # RN9617241 (Control No. 3558029)
Estado compacto: Licencia multiestatal: Autorizado para ejercer en 40 Estados*
Dr. Alex Jiménez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Mi tarjeta de presentación digital